Cours
du 18/10/00
Guillaume Radioactivité :¾
Spectres d’Emission et d’Absorption
Duc ¾
Radio isotope
¾
Rayonnement Gamma
I-/ A LA PERIPHERIE DU
NOYAU:
1-/
Généralités :
Un
élément quelqu’il soit est caractérisé par 2 valeurs :
A ® Nombre de Masses º Nombre de nucléons N
Z ® Numéro Atomique º Nombre de protons
º Nombre d’électrons orbitaux
(l’atome étant a priori neutre)
Þ Z caractérise respectivement, à la fois, un paramètre nucléaire et atomique
Les électrons gravitent autour du noyau central sur des orbites parfaitement définies qui ont chacune une énergie, elle aussi parfaitement définie qu’on appelle l’énergie orbitale, Eorb
2-/ Caractéristiques de l’Eorb :
- Par convention, l’énergie orbitale est strictement négative : Eorb < 0
- Elle est d’autant plus petite(en valeur absolue) que l’on s’éloigne du noyau de telle façon qu’elle devienne nulle lorsqu’on est à l’infini ; les énergies les plus élevées étant donc plus proches du noyau.
- Elle peut être facilement calculer par la formule suivante :
E(n) = - E(o) Z²/n²
Avec E(n) : Energie
n: nombre quantique de
la couche
Z : nombre atomique de
l’élément considéré
E(o) = 13.6eV : Energie de la première
couche de l’atome d’Hydrogène(Z=1, A=1)
1eV = 1,60 x 10^-19J
Plus
l’élément est lourd, plus Z est élevé et plus l’Eorb est élevée des couches les
plus profondes aux couches les plus superficielles.
Tableau d’Eorb en keV :
|
Z |
Eléments |
Couche K (KeV) |
Couche L (KeV) |
|
1 |
H |
- 0,0136 |
|
|
20 |
Ca |
-
4,36 |
-
0,399 |
|
74 |
Tu |
-
69,508 |
-
12,09 |
|
82 |
Pb |
-
88,001 |
-
15,87 |
N.B : Tu ® Tungstène, anticathode des tubes à RX
Pb ® Plomb, permet de protéger des radiations
3)L’énergie
de liaison :
Pour arracher un électron de sa couche, il faut fournir El = Energie de liaison de l’électron
-
El > 0
-
El = Eorb au signe près
-
Elle
décroît quand on s’éloigne du noyau
II-/PHENOMENES D’EXCITATION:
1)Paradoxes :
L’électron
est donc sur une couche déterminée à l’Eorb,
E(n) déterminée. Or, a priori, il tourne sur cette orbite, la mécanique
quantique nous dit, à l’opposé de celle classique, que malgré son mouvement, il
ne perd pas d’énergie, le système reste stable, l’électron ne va pas ralentir
et s’écraser sur le noyau.
Cet
électron, il faut le choisir pour essayer de le déterminer. Si l’on veut le
voir, i.e déterminer sa localisation, on ne peut pas savoir sa vitesse et
inversement. Donc on ne peut avoir les deux informations en même temps.
2)Emission-Absorption :
Le
déplacement d’un électron d’une orbite i à j entraîne soit l’émission soit l’
absorption d’énergie telle que : E(ij) = hn = Ei-Ej
Avec
h = Constante de Planck = 6,62 x 10^-34 J . s
n = Fréquence du rayonnement
en Hz ou s-1
Exemple : Dans l’atome d’hydrogène,
H(Z = 1, A = 1) à l’état fondamental l’électron est sur la couche K (n=1)
Energies
orbitales des différentes couches :
N
E en eV
1
E(1) = -13.6 eV
2
E(2) = -13.6.1²/2² = -3.39 eV
3
E(3) = -13.6/9 = -1.51 eV
5
E(5) = -13.6/25 = -0,54 eV
Supposons
que l’atome d’Hydrogène reçoive de l’énergie, il est excité et que son électron
passe de la couche 1 à 5 :
E1/5 =
E1-E5 = -13,6-(-0,54) = -13,06 eV <0 Þ absorption d’énergie
ÞPour faire passer un
électron des couches profondes à superficielles, il faut fournir de l’énergie,
d’où le signe négatif de cette énergie.
Si
au contraire, lors d’une chute de la couche 5 à la couche 2:
E5/2 = E5-E2 = -0,54-(-3,39) = 2,85 eV >O Þémission d’énergie sous la forme d’un rayonnement
Il
y a émission d’un photon, d’une radiation, c’est l’origine des RX qui sont en
partis dus au déplacement des électrons des couches superficielles vers les
profondes.
3)Spectres
d’émission ou d’absorption :
On
définit donc un spectre d’absorption et
d’émission. Tous les cas étant possibles, l’électron pouvant sauter ou chuter
de sa couche vers n’importe qu’elle autre. On aura alors les photons
correspondant.

III-/LE RADIOISOTOPE :
Il
existe des radioéléments, éléments instables car ayant un excès d’énergie par
rapport à leur état fondamental. Il libère spontanément cette énergie pour
retourner à son état fondamental en émettant un rayonnement caractéristique.
1/ Généralités
_Radio,
car radioactif caractérisé par l’émission d’un rayonnement
_Isotope
car élément aux caractéristiques particulières même Z mais A différent de
l’élément stable correspondant.
_Leur
radioactivité est de nature nucléaire. Les radioéléments sont instables, dû à
un excès d’énergie par rapport à leur état fondamental. Ils la libèrent
spontanément sous la forme d’un rayonnement pour la retrouver.
_Chaque
élément est déterminé par des valeurs A et Z ( cf infra). On connaît 282 à300
éléments stables et plus de 600 radioactifs.
He( 4;2) A=4 Z=2 N=2
U(238;92 ) A=238 Z=92 N=146
On
constate que plus l élément est lourd plus il faut de neutron pour assurer la
stabilité ( prés de 2 fois plus pour l’uranium).
2/
Radioactivité
_
phénomène nucléaire à l’origine de l’émission de radiation
découverte
par H.Becquerel le 01/03/1896 prix Nobel de physique en 1903 ( HB et Pet M
curie)
_
Electromagnétique : gamma g
N.B :
de même nature que le RX mais appelé X si d’origine orbitale et g si d’origine nucléaire.
Particules
chargées : a b+ b- ions lourds
Particules
neutres : neutrons n, assez lourd
neutrino n, particule légère et sans charge.
Corps instable ® corps stable + rayonnement
X ® X’ + rayonnement a,b-,b+,g ,n,n
_Ces rayonnements sont exactement égaux à la différence d’énergie fondamentale entre le corps X et X’.
_On
constate qu’il existe de nombreuses configurations du nombre de proton et de
neutron au sein du noyau.
3/ Energie de liaison
_Au
niveau du noyau il y a Z protons
chargés positivement et N neutrons neutres
Qu’
est ce qui explique que les particules chargées ne se repoussent pas et restent
liées ?
_Les
nucléons sont liés entre eux par une énergie de liaison.
Si l’on prend un corps X(A ;Z) A nucléons ,Z
protons ,A-Z neutrons
_ A priori : mX(A ; Z) = Zmp + ( A-Z)
mn
Or mX(A ;Z) < å m
nucléons
Dm = somme m nucléons – m
X(A ;Z) =défaut de masse
_C’est
l’équivalent en énergie de ce défaut de masse sous la forme DE=c²Dm qui est l’énergie de
liaison qui fera que
le noyau reste lié, existe donc constitue des corps stables ou instables
DE = Energie à fournir au
noyau pour le séparer en ses éléments
DE = Energie libérée quand Z
proton et N neutron se réunissent pour former un noyau
_B
=(DE)/A ® Energie de liaison moyenne
par nucléon
4/ Exemple de l’uranium : U(235;92 ) Z=92 ,N=143
_
On raisonne toujours en unité de masse atomique ( uma )
1 uma = 1.66 10^(-27) kg
m U (235; 92) = 235.043915 uma
m p =1.00727 uma
m n = 1.00866 uma
Dm= (Zmp+Nmn) – mX(A;Z)
= (92x1.00727+143x1.00866) - 235.043915
=
236.90722 - 235.043915
Dm= 1.863305 uma
El=
Dm x 931.5= 1735.669 MeV
B= El / 235= 7.385824Mev
Þ L’énergie dans le noyau
pouvant être libérée est énorme.
5-/
courbe de l’énergie de liaison / nucléons tous les élément ou fonction de Z
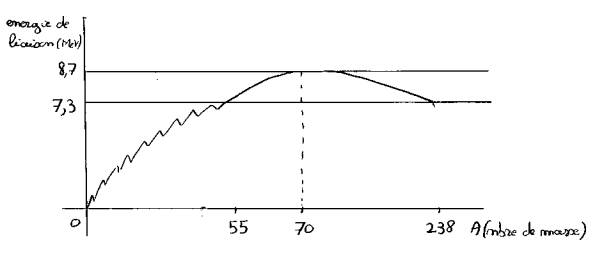
On
observe 3 segments à cette courbe
*1-/
[ 0 ;55] environ :
On y trouve les éléments léger aux énergie de liaison d’autant plus petites qu’ils sont légers avec une discontinuité pour les A paires : He Be C
Lorsqu’on
fusionne 2 noyaux légers on obtient un noyau plus stable, plus la libération
d’énergie, environ 6MeV/nucléon
H (2 ; 1) + H(2
;1) ® He (4 ; 2) + w
thermonucléaire
C’
est pourquoi la bombe thermonucléaire à hydrogène est infiniment plus nocive
que la bombe atomique faisant appel à la fission.
*2/Le
palier, vers Z @ [55 ;70] avec Bmax ~ 8.7 MeV :
Cela
concerne les éléments tels que : Ni Fe Co, i.e tous les éléments les plus
riches de la terre. Quand la Terre s’est formé, quelque soit le mode ( une
discontinuité® Big Bang ; ou un
continuum ), au début toutes les configurations possibles ont existé et
certaines étaient plus instables que d’autres. Ces premières ont
progressivement disparus, celles restant sont les plus stables; compte tenu de
l’âge de la terre il ne peut y avoir de radio-isotopes à l’heure actuelle, car
tous les radio-isotopes, qui sont des radioéléments, ont disparu vu cet âge. Les seul corps radioactifs naturels sont
ceux dont la période T, la demi vie, est proche de l’âge de la Terre@10^9 années. On utilise en médecine que les
radio-isotopes que l’on sait fabriquer.
3/
La décroissance Z>70
il
y a une diminution du Bmax jusqu’à
B=7.3 MeV pour U238 . Et c’est là où plus l’élément est lourd et plus il
est instable et donc plus il tend à se casser : la fission. Il peut le faire spontanément ou on peut l’aider
parce qu’il est a la limite de la stabilité et on peut alors libérer
1MeV/nucléon
noyau
assez lourd ®
fission ® 2
noyaux plus légers plus stables + W
La
fusion libère 6x plus d’énergie que la fission.
IV/ Rayonnements
1/Généralités
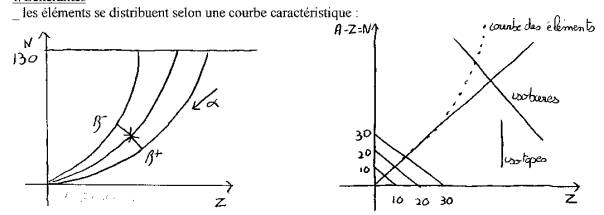
NB : configuration
instable avec n , p ou n et p élevés.
_
On constate que pour les éléments légers N=Z placer sur la bissectrice . plus
l’élément devient lourd et plus l’on s ‘écarte de la bissectrice, i.e qu’il
faut un nombre de neutron de plus en plus grand lorsque le nombre de proton
croît jusqu’à arriver à l’U(238 ; 92)
Donc
autour des éléments stables qui constituent cette distribution on a les
éléments radioactifs que l’on sait créer artificiellement.
-
Isotopes même Z, mais N #
-
Un Isobare possède un même nombre de masse A et un numéro atomique Z différent
de l’élément correspondant. (A est identique et Z diffère)
2)Les
3 grands types de désintégrations des corps radioactifs en corps stables :
- Isobarique :
b- , b+ , CE (Capture
Electronique)
X(A ; Z) ® X(A ; Z’) + r *
- Par
partition : a ( et phénomène de fission)
X(A ;Z) ® X(A’ ;Z’) + r *
- Gamma
g : Emission spontanée,
isomérie, CI(Conversion Interne)
X(A ; Z) ® X(A ; Z) + r *
3)Désintégration g :
Le
rayon g est créé par le noyau,
c’est un rayonnement électromagnétique, pour nous c’est essentiellement
le rayonnement du diagnostic, aussi utilisé en thérapeutique.
X(A ;
Z) ® X(A ;Z) + g
a)Emission spontanée : Durée de vie négligeable du corps excité
après
émission a ou b
Exemple : Du cobalt, la bombe à
Cobalt avec du Co (60 ; 27)
Exemple : Du cobalt, la bombe à
Cobalt avec du Co (60 ; 27)
Dans
la bombe au Cobalt, ce sont les 2 rayons g qui sont utilisés. Le
Cobalt * est très dangereux, s’il y a contact direct, avec la main par exemple,
les lésions seront importantes amenant des brûlures, des douleurs et
nécessitant une amputation. Ici,
l’émission des 2 rayons g est quasi immédiate de
celle du rayonnement b, on ne peut donc isoler le
Ni (60 ;28). C’est pourquoi le Co (60,27) n’est pas utilisé pour le
diagnostique.
b)Isomérie : Durée de vie du noyau excité longue,
permettant la séparation de
l’émetteur a ou b Exemple
du Technétium 99 Métastable (caractérisant l’isomérie ) On a donc des vaches à Technétium, une ampoule à
Molybdène, que l’on élue avec un liquide permettant d’entraîner le Tc (99m), et
on a le liquide avec uniquement du Tc (99m) que l’on peut injecter au patient. c)Conversion
Interne : - Photon g arrache un électron - Effets secondaires : Photons X et
électron Auger Le
noyau se désintègre par émission g , mais pour certains corps
le rayonnement g va rentrer en collision
avec un électron périphérique et si son énergie est supérieure à l’énergie de
liaison de l’électron, il va l’arracher et créer un trou dans cet atome. On
a donc un photon g ajouté à cela un électron
dit Auger dangereux pour l’organisme. De plus, il va y avoir chute des
électrons périphériques pour combler le trou laisser par la collision, et donc
émission d’un ou plusieurs photon X. Þ On n’utilise jamais de
corps radioactifs dont on sait qu’ils se désintègrent sous forme de rayonnement
g accompagné du phénomène de Conversion
Interne (CI)
b

Le rayonnement b est exceptionnellement utilisé par
irradiation à l’extérieur, car son parcours dans le tissu est extrêmement
court.

T Tc (99m) = 6h , on a donc tout le temps de le séparer du Molybdène

